Química · Formulación
Hidruros Metálicos: Nomenclatura, Ejemplos y Test
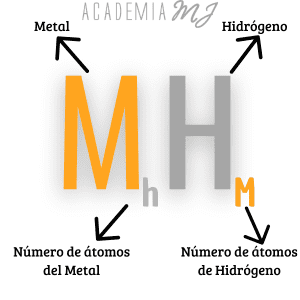
Son la combinación del Hidrógeno con un metal. Se expresa con la siguiente fórmula:
¿Ya te lo sabías y no necesitas explicación?
¡Pues practica rellenando esta tabla en PDF descargable!
↓
Reglas IUPAC
Metal + Hidrógeno
¿Cómo nombrar los hidruros metálicos?
En estos compuestos, el hidrógeno actúa con estado de oxidación -1. Su nomenclatura es sencilla si conoces las valencias del metal.
1) Nomenclatura Sistemática (Prefijos)
Utilizamos prefijos griegos (mono-, di-, tri-) para indicar el número de hidrógenos.
Ejemplo:
CaH₂
→ dihidruro de calcio
2) Nomenclatura de Stock
Indicamos la valencia del metal en números romanos entre paréntesis (solo si tiene más de una).
Ejemplo:
FeH₃
→ hidruro de hierro (III)
| Fórmula | Nomenclatura Sistemática | Nomenclatura de Stock |
|---|---|---|
| LiH | Hidruro de litio | Hidruro de litio |
| NaH | Hidruro de sodio | Hidruro de sodio |
| CaH₂ | Dihidruro de calcio | Hidruro de calcio |
| AlH₃ | Trihidruro de aluminio | Hidruro de aluminio |
| FeH₂ | Dihidruro de hierro | Hidruro de hierro (II) |
| PbH₄ | Tetrahidruro de plomo | Hidruro de plomo (IV) |
Práctica
Ejercicios aleatorios
Test online hidruros metálicos
Completa los campos que faltan. Pulsa Verificar y revisa tu puntuación.
| Fórmula | N. sistemática (prefijos) | Nomenclatura de Stock |
|---|
Material relacionado
Creo que esto te puede interesar bastante.
Preguntas frecuentes sobre Hidruros Metálicos
1. ¿Qué son exactamente los hidruros metálicos?
Son compuestos binarios formados por la unión de un metal con el hidrógeno. En esta combinación, el hidrógeno actúa con estado de oxidación -1 (ion hidruro, H⁻). Suelen ser sólidos cristalinos con un marcado carácter iónico.
2. ¿En qué se diferencian de los hidruros volátiles?
La principal diferencia es el tipo de enlace y el elemento acompañante. Los hidruros metálicos presentan enlaces iónicos y metales, mientras que los hidruros volátiles son compuestos moleculares covalentes formados con no metales de los grupos 13, 14 y 15.
3. ¿Qué nomenclatura es preferible usar en un examen de Química?
Ambas son válidas, pero la clave es la precisión:
- Nomenclatura Sistemática: Es la más segura si no te quieres complicar con las valencias (ej: dihidruro de calcio).
- Nomenclatura de Stock: Es muy común en exámenes. Recuerda indicar la valencia en números romanos solo si el metal tiene más de una (ej: hidruro de hierro (II)).
4. ¿Cómo sé qué valencia usar para cada metal?
Es fundamental dominar los estados de oxidación de los metales alcalinos (+1) y alcalinotérreos (+2). Para no fallar nunca, te recomendamos consultar nuestra Tabla Periódica Dinámica, diseñada específicamente para ayudarte con la formulación.
5. ¿Por qué la mayoría de los hidruros metálicos son sólidos?
Debido a su estructura de red iónica. La fuerte atracción electrostática entre los cationes del metal y los aniones hidruro (H⁻) requiere mucha energía para romperse, lo que resulta en puntos de fusión altos y estado sólido a temperatura ambiente.
6. ¿Se pueden confundir con los hidrácidos?
Aunque ambos llevan hidrógeno, son opuestos. Los hidrácidos (como el HCl) son no metales con hidrógeno y tienen carácter ácido en agua. Los hidruros metálicos son metales con hidrógeno y, al reaccionar con agua, suelen liberar gas hidrógeno y formar hidróxidos básicos.
7. ¿Cuál es el error más "típico" al formular estos compuestos?
El error estrella es olvidar que el símbolo del metal siempre va a la izquierda y el del hidrógeno a la derecha (ej: LiH, nunca HLi). También es frecuente confundir la valencia del metal al intercambiar subíndices.